Заболеваемость
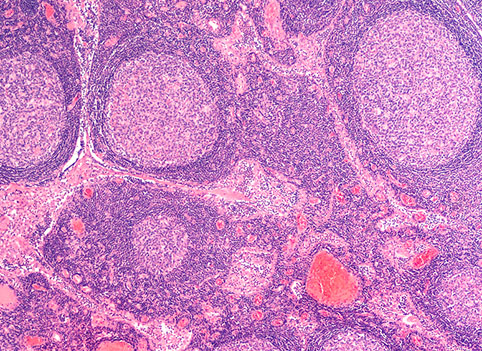
Фолликулярные лимфомы представляют второй по частоте встречаемости подтип нодальных злокачественных лимфом. Заболеваемость быстро повышается на протяжении последних десятилетий и с 1950 года увеличилась с 2-3 случаев на 100 тыс. чел. в год до 5-7 случаев на 100 тыс. чел. в настоящее время.
Диагноз
Диагноз устанавливается по результатам эксцизионной биопсии лимфоузла.
Игольную биопсию следует выполнять только больным с поражением трудно доступных лимфоузлов (например, забрюшинные лимфоузлы). Тонкоигольная биопсия недостаточна для постановки достоверного диагноза.
Гистологический диагноз устанавливается в соответствии с критериями текущей классификации ВОЗ. Стадирование выполняется в соответствии с числом бластных клеток в поле зрения (1-2 цитологическая степень 1-2: <15 бластов, 3 цитологическая степень: >15 бластов).
Фолликулярная лимфома 3б цитологической степени (только бластные клетки) расценивается как агрессивная лимфома и лечение этой формы заболевания должно проводиться в рамках клинических исследований, разработанных для диффузной В-крупноклеточной лимфомы (ДВКЛ, см. соответствующий раздел).
Дополнительный гистологический материал, при наличии, рекомендуется подвергнуть глубокой заморозке для дальнейшего выполнения дополнительного молекулярного анализа (исследование в настоящее время все еще представляет сугубо научный интерес).
Стадирование и оценка прогноза
Поскольку терапия в значительной степени определяется стадией заболевания, необходимо тщательно стадировать процесс исходно, особенно важно выявление больных с начальными I и II стадиями (15-20%).
Первичное обследование должно включать КТ-исследование грудной клетки, брюшной полости и малого таза, аспирацию и биопсию костного мозга.
В соответствии с последним консенсусом дополнительное выполнение ПЭТисследования с целью стадирования не рекомендуется, и исследование показано только в редких случаях для подтверждения локализованного процесса при I/II стадиях [IV,C].
Лабораторные исследования включают развернутый анализ крови с подсчетом лейкоцитарной формулы, биохимический анализ с определением уровня ЛДГ, мочевой кислоты, а также обязательные исследования на ВИЧ-инфекцию, гепатиты В и С.
Стадия устанавливается в соответствии с классификацией Ann Arbor с указанием локализации массивного (“bulky”) поражения.
Для оценки прогноза рекомендуется определять международный прогностический индекс, разработанный специально для фолликулярных лимфом ― FLIPI, который учитывает следующие факторы: поражение >4 зон лимфоузлов, повышенный уровень ЛДГ, возраст >60 лет, распространенная стадии III/ IV, гемоглобин <12 г/дл) [I,А]. Недавно была предложена пересмотренная версия FLIPII, включающая b2-микроглобулин, диаметр наибольшего лимфоузла, наличие поражения костного мозга и уровень гемоглобина.
Анализ экспрессии генов на уровне РНК говорит о более благоприятном клиническом течении при наличии Т-клеточной инфильтрации, по сравнению со случаями обогащенными неспецифическими макрофагами. Данная техника, однако, еще не вполне применима для рутинной клинической практики.
Лечение
Стадия I-II
Для небольшого числа больных I-II стадией потенциально излечивающей может быть лучевая терапия (ЛТ), которую следует проводить расширенными полями (30-40 Гр) [II, B].
Для пациентов с большой опухолевой массой (“bulky”), перед проведением лучевой терапии также может быть использована системная терапия, применяемая при распространенных стадиях [IV,B].
Стадия III-IV индукция
Для большей части пациентов с распространенными III и IV стадиями излечивающей терапии в настоящее время не существует [II, B]. Поскольку естественное течение болезни характеризуется спонтанными регрессиями в 15-20% случаев и варьирует от случая к случаю, химиотерапию следует начинать только при появлении В-симптомов, вовлечении гемопоэтической ткани, наличии “bulky” или быстром прогрессировании лимфомы [I,А].
Если целью терапии являются полная ремиссия или длительная безрецидивная выживаемость терапией выбора служат ритуксимаб в комбинации с химиотерапевтическими режимами: СHОР (циклофосфан, доксорубицин, винкристин и преднизолон), СVР, комбинации на основе пуриновых аналогов (FC или FM, бендамустин) [I,B]. Добавление ритуксимаба к химиотерапии улучшает показатели общего ответа, безрецидивную и общую выживаемость, что было подтверждено в четырех проспективных клинических исследованиях терапии первой линии, в двух исследованиях «терапии спасения» и по данным мета-анализа.
Монотерапия моноклональными антителами (ритуксимаб, радиоиммунотерапия) или монотерапия алкилирующими препаратами является альтернативой для пациентов низкого риска или при наличии противопоказаний к проведению более интенсивной химиоиммунотерапии [III, B].
Стадия III-IV консолидация
Мета-анализ говорит о незначительном улучшении выживаемости больных при проведении поддерживающей терапии интерфероном–., назначение которого должно быть противопоставлено ожидаемой токсичности.
Поддерживающая терапия ритуксимабом в течение 2-х лет увеличивает время до прогрессирования (PFS) [I, B].
Радиоиммунотерапия улучшает показатели времени до прогрессирования (PFS), однако преимущество данного метода после применения ритуксимабсодержащих индукционных режимов установлено не было [I,B].
Миелоаблативная химиолучевая терапия с последующей трансплантацией аутологичных стволовых клеток увеличивает время до прогрессирования (PFS), но не общую выживаемость (OS), как было показано в четырех рандомизированных клинических исследованиях, и, таким образом, не может быть рекомендована в качестве стандарта лечения вне рамок клинических исследований [I, А].
Рецидив заболевания
Для исключения вторичной трансформации в агрессивную лимфому рекомендовано выполнение повторных биопсий.
Выбор терапии второй линии зависит от эффективности предшествующего режима. При ранних рецидивах (<12 месяцев), предпочтительно применение схем химиотерапии, не обладающей перекрестной резистентностью (например, флударабин после СНОР). Повторное использование ритуксимаба во второй линии рекомендуется в случае длительности первой ремиссии более 6 месяцев после использования препарата в первой линии [I,А].
Радиоиммунотерапия представляет собой эффективный терапевтический подход, особенно в группе пожилых, соматически отягощенных пациентов, при наличии противопоказаний для проведения химиотерапии. В остальных случаях метод может применяться с целью консолидации.
Поддерживающая терапия ритуксимабом продолжительностью до 2-х лет не обладает выраженными побочными эффектами и, как показал системный мета- анализ, существенно увеличивает время до прогрессирования (PFS) и показатель общей выживаемости (OS) при лечении рецидивов, даже после ритуксимаб- содержащей индукционной терапии [I,А].
Миелоаблативная консолидация с последующей трансплантацией аутологичных стволовых клеток увеличивает длительность времени до прогрессирования, показатели общей выживаемости, однако ее роль в эру ритуксимаба требует пересмотра [I,B].
Может быть рассмотрено применение потенциально излечивающей трансплантации аллогенных стволовых клеток (в том числе с кондиционированием пониженной токсичности).
Оценка эффективности
Адекватное радиологическое исследование должно проводиться в процессе и после завершения химиотерапии. Для незамедлительного проведения терапии «спасения» необходимо раннее выявление пациентов в неполной ремиссии или с отсутствием ответа.
Наблюдение
Сбор анамнеза и физикальный осмотр должны проводиться один раз в 3 месяца на протяжении первых 2 лет, каждые 4-6 месяцев в течение последующих 3 лет и затем один раз в год; при этом внимание должно акцентироваться на возможности трансформации в агрессивную лимфому и вероятности развития вторичных опухолей, включая острые лейкозы [V,D].
Анализ крови выполняется каждые 6 месяцев в течение первых 2-х лет и далее только при появлении подозрительных симптомов.
У пациентов, получавших лучевую терапию на область шеи на первом, втором и пятом годах наблюдения должна проводится оценка функции щитовидной железы.
Минимальный радиологический или ультразвуковой контроль должен быть проведен 1 раз в 6 месяцев на протяжении первых 2-х лет и далее ежегодно однократно.
Мониторинг минимальной резидуальной болезни (MDR) может быть выполнен в рамках клинических исследований, однако не должен быть основой планирования лечебной тактики.








